Hemoglobin
Barviva, která se vyskytují v lidském těle, jsou po chemické stránce velice různorodá. Nejdůležitějšími z nich jsou pyrolová barviva. Jedním z nejdůležitějších pyrrolových barviv je porfyrin, který vznikají náhradou vodíku v pyrrolových jádrech. Dále mohou také vznikat uroporfyriny, koproporfyriny aj.. Tyto sloučeniny se od sebe liší pouze svými radikály. Schématicky můžeme tyto sloučeniny znázornit takto:
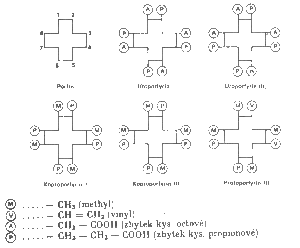
Porfyrin
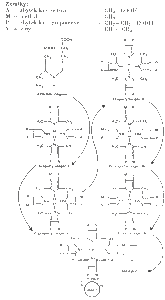
Syntéza porfyritů a krevního barviva
Studium látkové výměny hemoglobinu ukazuje, že všechny jeho součásti vznikají znovu při syntéze erytrocytů. Využité bílkoviny červených krvinek se odbourají na aminokyseliny a hem z hemoglobinu se vyloučí ve formě žlučového barviva. Syntéza hemu je spojena se syntézou porfyritového kruhu. V hemoglobinu a bílkovinách obsahujících hem (myoglobin a cytochrom c) se vyskytuje tentýž hem. Chemií protoporfyrinu se zabýval H. Fischer, který popsal i jeho syntézu.
Protoporfyrínový skelet se skládá ze 4 pyrrolových kruhů a 4 methinových skupin. Z tohoto skeletu vznikne protoporfyrin substitucí 8 radikály.
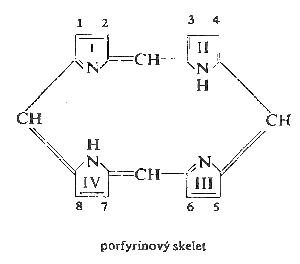
Porfyrinový skelet
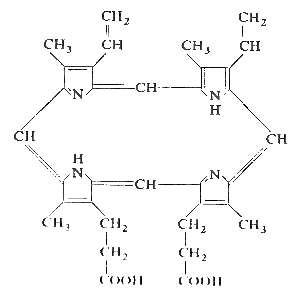
Porfyrit, který je obsažen v hemu hemoglobinu, obsahuje 3 odlišné substituenty na uvedených 8 místech. Těmito substituenty jsou dva vinylové zbytky, dvě propionové kyseliny a čtyři methylové skupiny. Z toho vyplívá, že v daném případě je možných 15 různých izomerů, které obsahují tyto skupiny v různém pořadí. H. Fischer tyto izomerní možnosti označil číselně a zjistil, že protoporfyrin obsažený v hemoglobinu odpovídá protoporfyrinu IX, jehož složení je 1,3,5,8 – tetramethyl – 2,4 – divinyl – 6,7 – dipropionyl – porfin.
Protoporfyrin IX
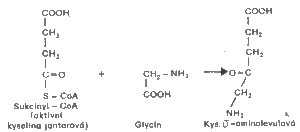
Při studiu syntézy hemu bylo zjištěno, že nejdříve vzniká kyselina d – aminolevulová (ALA). Tato kyselina vzniká kondenzací sukcil – CoA a glycinu za vzniku teoretické sloučeniny kyseliny a – amino – b – ketoadipové. Tato sloučenina dekarboxyluje za vzniku kyseliny d – aminolevulové. Celý proces katalyzuje d – aminolevulátsyntetáza (ALA – syntetáza). Dále je při této reakci nutná přítomnost pyridoxal fosfátu, který je aktivátorem gylicinu. Tato reakce probíhá pouze v mytochondriích savců.
Dalším článkem syntézy hemu je syntéza porfobilinogenu (PBG). Při této reakci katalyzované enzymem ALA – dehydrogenásou, se spojují dvě molekuly ALA za vzniku pyrolového derivátu porfobilinogenu
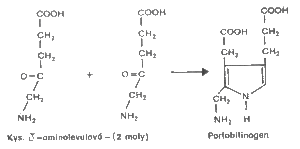
Porfobilinogen
V reakci následuje syntéza uroporfyrinogenu. Ten vzniká spojením 4 porfobilinogenů. Tímto spojením vzniká tetrapyrolové jádro uroporfyrinogenu. Toto spojení se odehrává za ztráty čtyř molekul amoniaku za přítomnosti PBG – deaminasy (uroporfyrinogen – I – syntetázy). Podle uspořádání postraních řetězců (acetyl nebo propionyl) rozlišujeme porfyrinogeny typu I nebo III. Jen typ III podléhá změnám, které vyúsťují ve vytvoření hemu. Tato transformace je katalyzována uroporfyrinogenásou
Další fází reakce je syntéza koproporfyrinogenu. Ten vzniká jako produkt dekarboxylace 4 acetylových radikálů na radikály methylové za přítomnosti uroporfyrinogendekarboxylasy.
Následuje reakce kterou vzniká protoporfyrinogen. Tato reakce probíhá tak, že současně dochází k oxidaci a dekarboxylaci 2 zbytků kyseliny propionové na zbytky vinylové za vzniku protoporfyrinogenu.
Následně dochází k transformaci protoporfyrinogenu na protoporfyrin za ztráty 6 protonů. 4 protony pocházejí z methylenových můstků 2 jsou přenášeny dusíkem pyrolových jader.
K dokončení syntéza hemu syntézy hemu dochází za přítomnosti hen syntetázy nebo ferochromchelasy, které zabudují atom Fe2+ do protoporfyrinového jádra. Nakonec se dokončí syntéza prstence hemu. Na syntézu každého prstence je třeba 8 molekul glycinu a 8 molekul kyseliny jantarové.